- Головна
- Готові шкільні презентації
- Презентація на тему «Періодична система»
Презентація на тему «Періодична система»
1262
Слайд #1
Періодична система

Слайд #2
В історії розвитку науки відомо багато великих відкриттів. Але деякі з них можна співставити з тим, що зробив Менделєєв - найвидатніший хімік світу. Хоча із часу відкриття його закону пройшло багато років, ніхто не може сказати, коли буде до кінця зрозумілий весь зміст знаменитої «таблиці Менделєєва».

Слайд #3
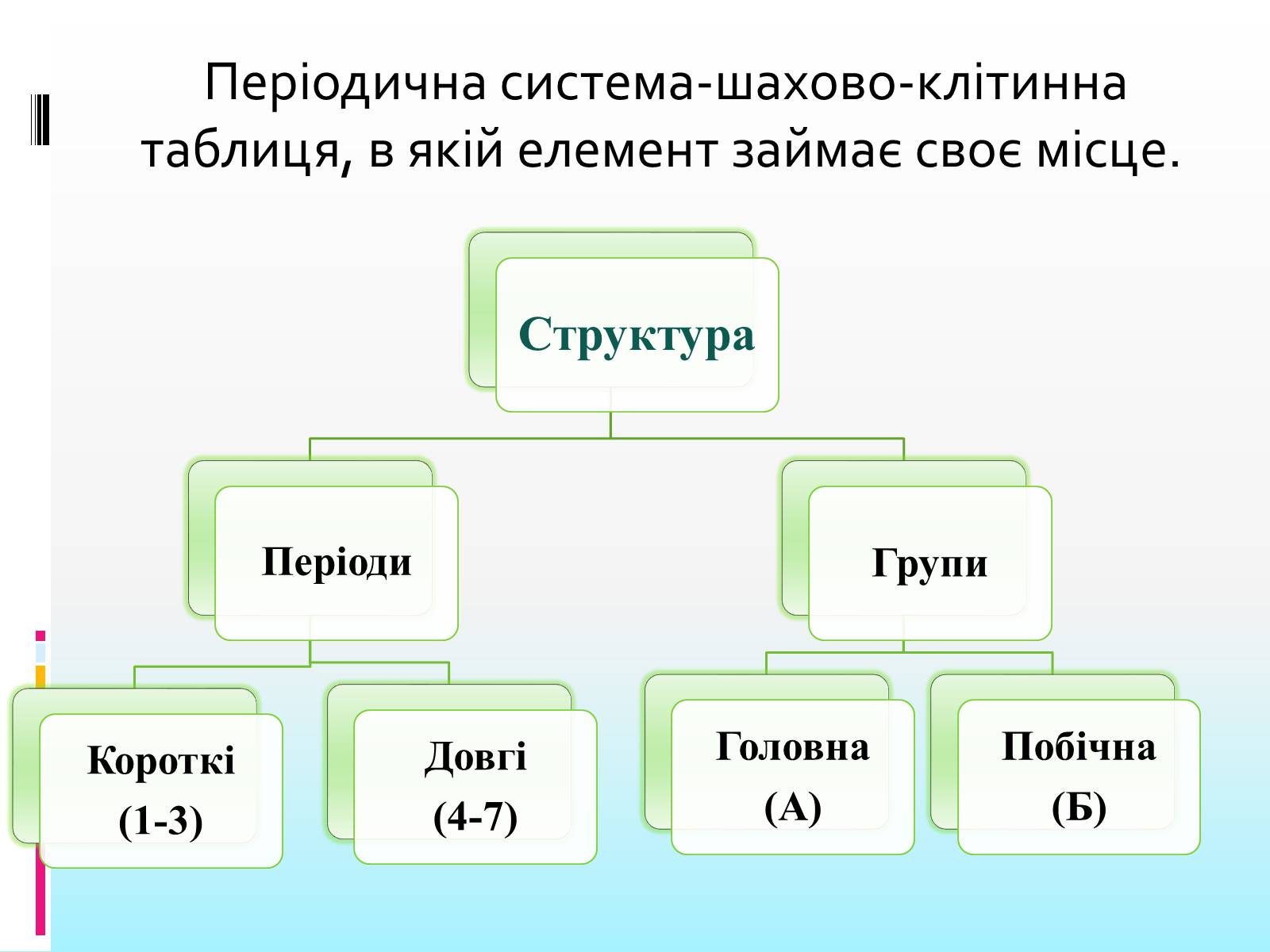
Періодична система-шахово-клітинна таблиця, в якій елемент займає своє місце.
Слайд #4
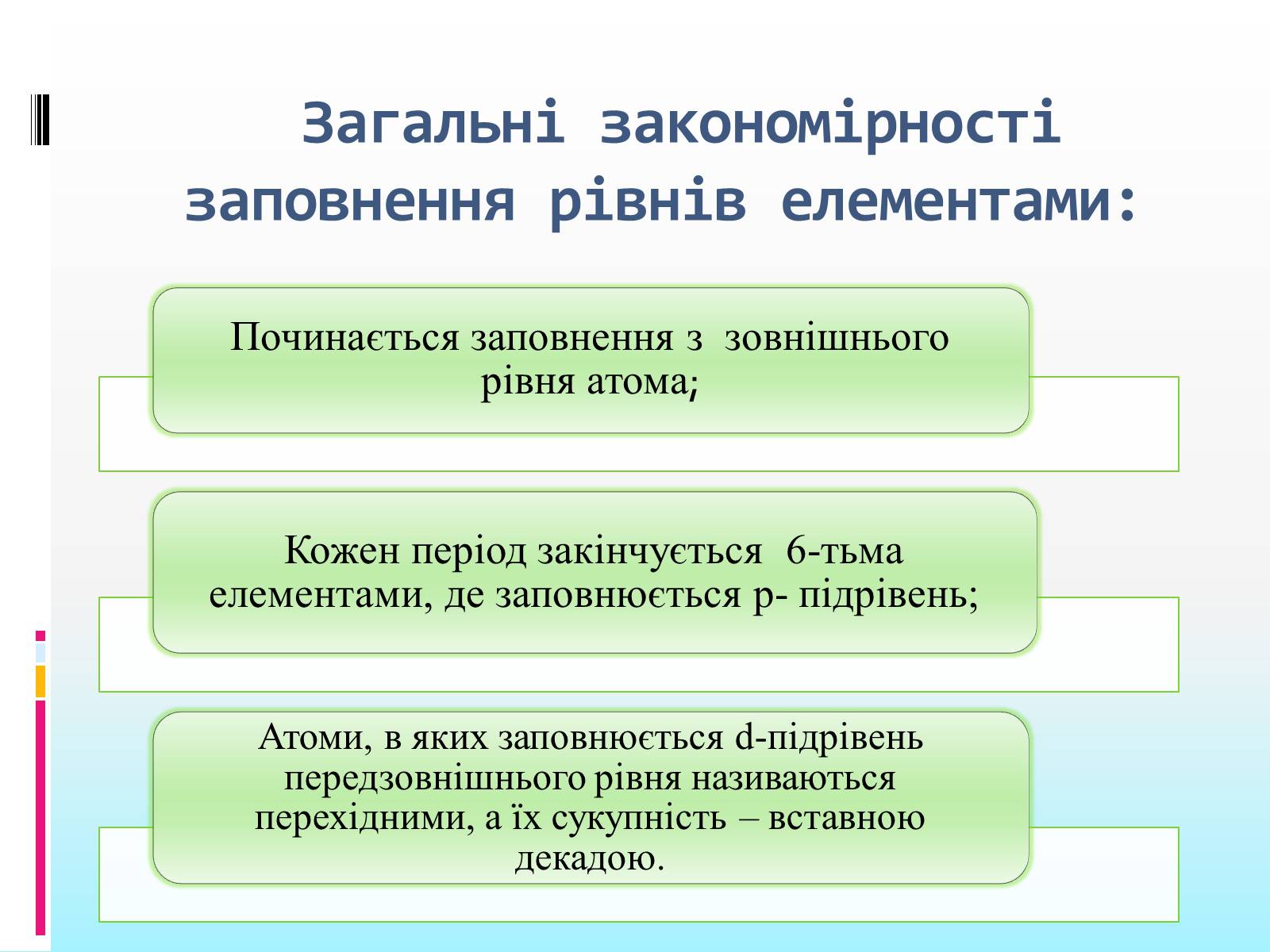
Загальні закономірності заповнення рівнів елементами:
Слайд #5
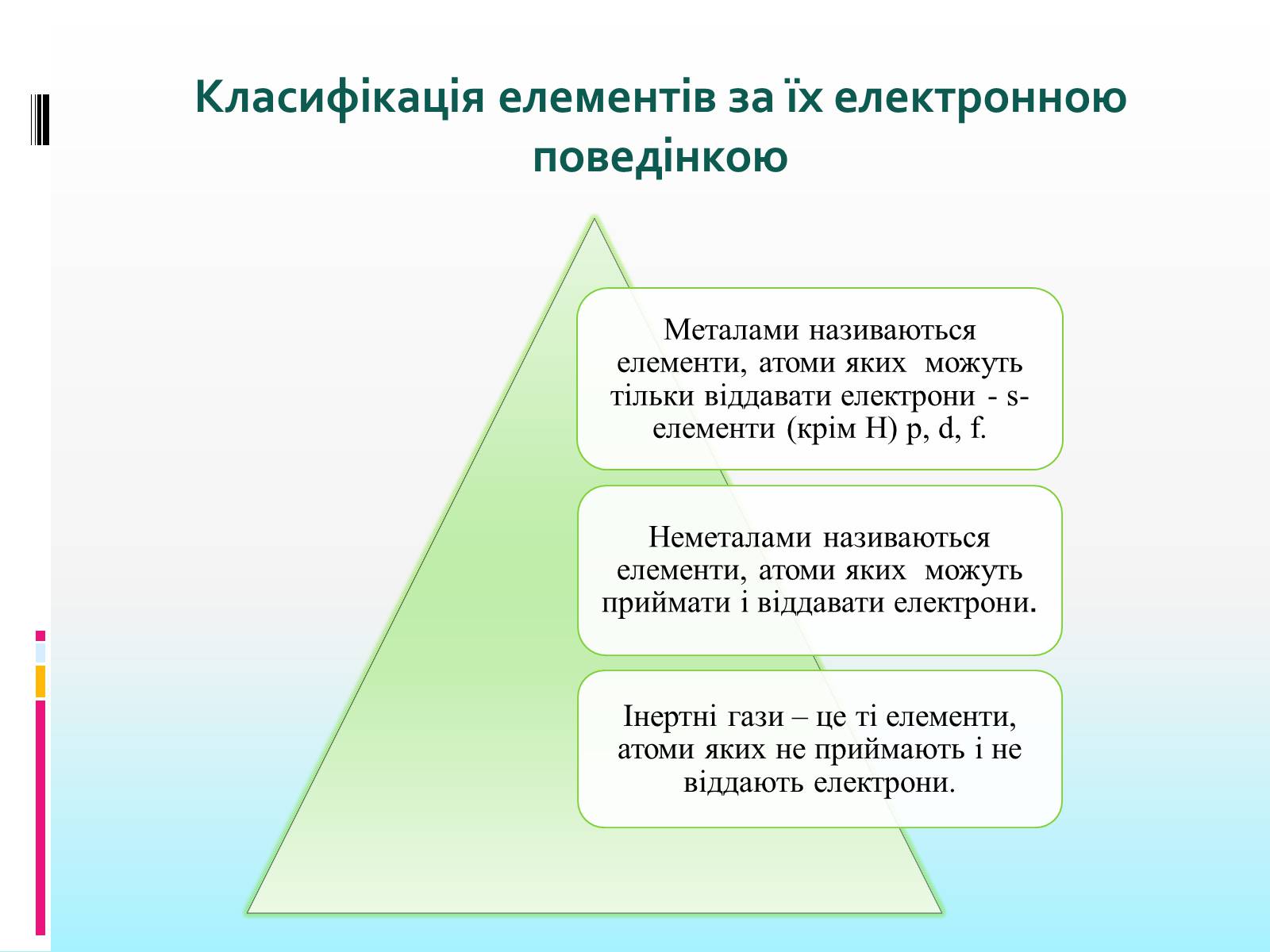
Класифікація елементів за їх електронною поведінкою
Слайд #6
Радіуси атомів (ефективний радіус атома) – це границя силового поля, ближче якої даний атом не підпускає ніякі інші частинки. В періодах r еф. зменшується, бо чергові електрони стають на один і той самий рівень, а Z весь час зростає. В А- підгрупах зверху вниз r еф. зростає, оскільки збільшується число електронних рівнів.

Слайд #7
Кількісна характеристика хімічних властивостей елементів

Слайд #8
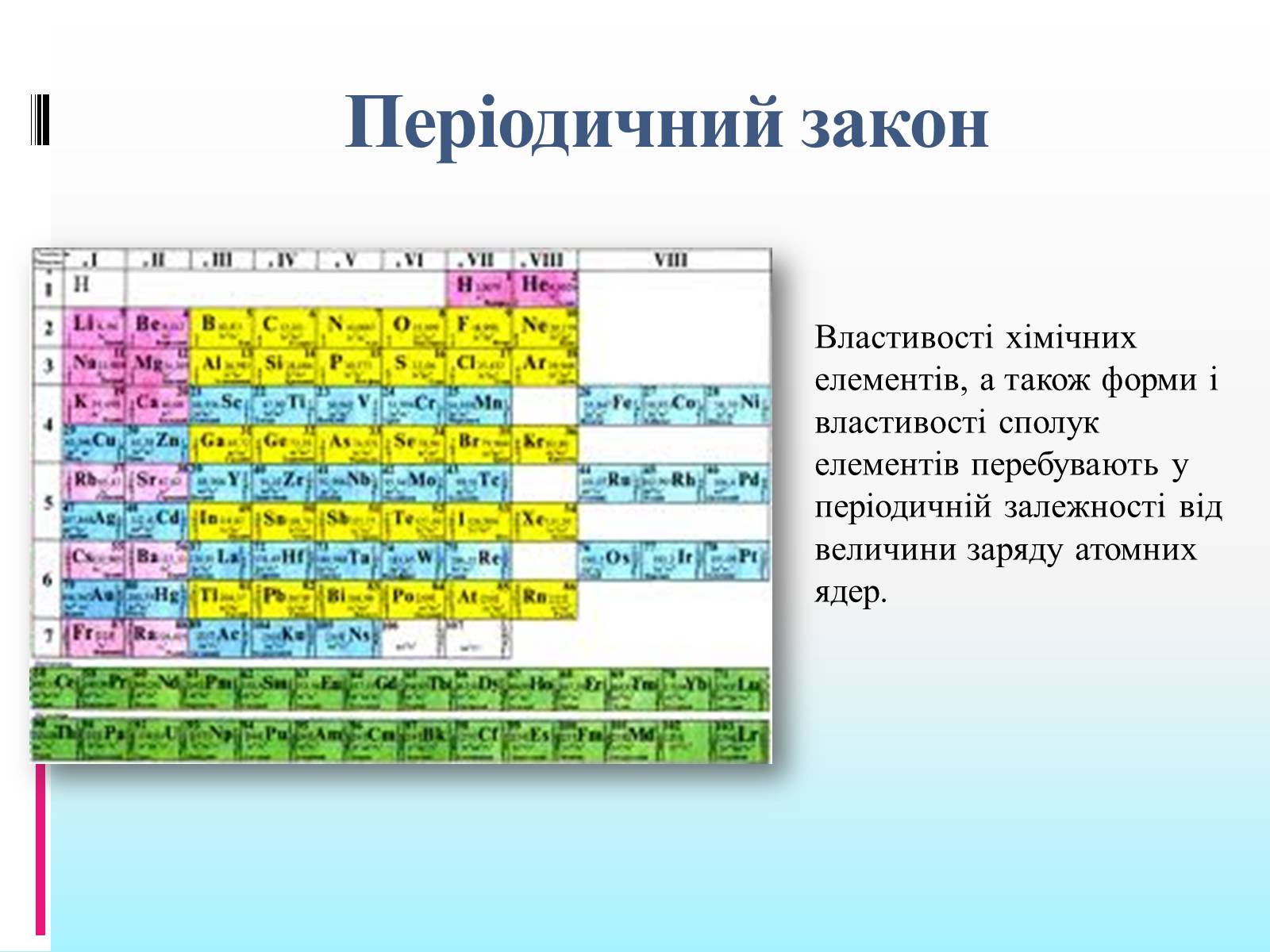
Періодичний закон
Властивості хімічних елементів, а також форми і властивості сполук елементів перебувають у періодичній залежності від величини заряду атомних ядер.
Властивості хімічних елементів, а також форми і властивості сполук елементів перебувають у періодичній залежності від величини заряду атомних ядер.
Слайд #9
В даний час поширеними є три форми таблиці Менделєєва: «коротка», «довга» і «наддовга».

Слайд #10
Вісім родин хімічних елементів
Слайд #11
Принципи заповнення Таблиці періодичної системи

Слайд #12
Електрон, як енергетична система, має власну кваркову структуру, тому при приєднанні до атома одночасно займає вісім точок простору, яким передає свою енергію. При цьому змінюється геометрична форма просторової будови атома.
Слайд #13
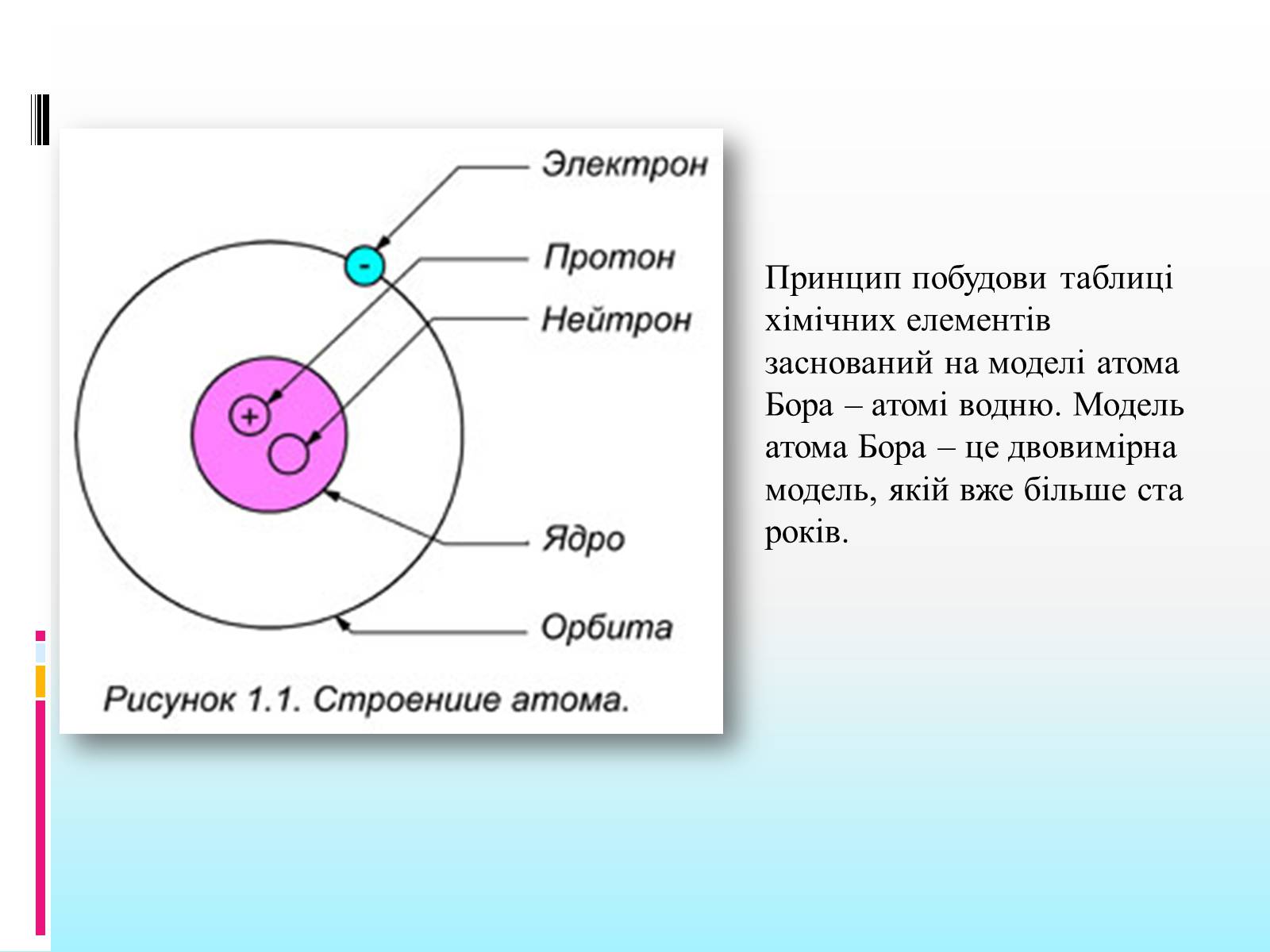
Принцип побудови таблиці хімічних елементів заснований на моделі атома Бора – атомі водню. Модель атома Бора – це двовимірна модель, якій вже більше ста років.
Слайд #14
Найменші матеріальні частки
Слайд #15
Електрон – енергетична частка, утворена з кварка простору під час первинного нуклеосинтезу. Електричний заряд електрона є одиничним випробувальним зарядом і дорівнює -1. Розмір електрона близько 2,8 x10 (-15) м.

Слайд #16
Нейтрон – енергетична частка реального навколишнього Всесвіту, утворена з 8 кварків простору вимірювання , що мають власну внутрішню структуру.Структура нейтрона або внутрішня організація електромагнітного поля елементарної енергетичної частинки є єдиною основою, на якій побудований весь матеріальний Всесвіт у всіх його просторових вимірах.

Слайд #17
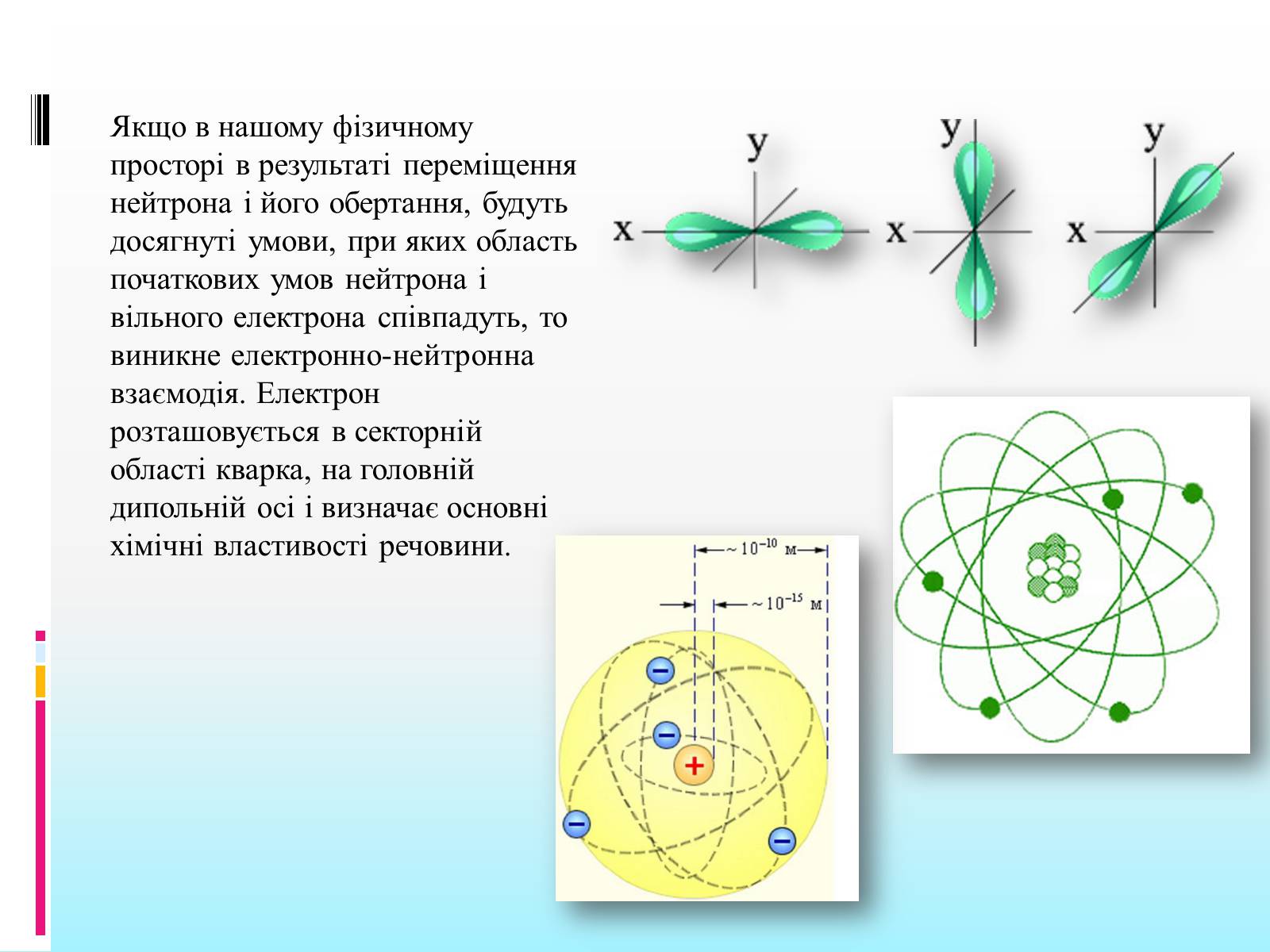
Якщо в нашому фізичному просторі в результаті переміщення нейтрона і його обертання, будуть досягнуті умови, при яких область початкових умов нейтрона і вільного електрона співпадуть, то виникне електронно-нейтронна взаємодія. Електрон розташовується в секторній області кварка, на головній дипольній осі і визначає основні хімічні властивості речовини.
Слайд #18
Конструкція кожного наступного за номером елементу включає в себе конструкцію попереднього елементу. Останнім елементом є елемент з порядковим номером 120, який має максимальну відносну масу А = 320. Всього хімічних елементів в природі є 120. Із них: s – елементів – 16; p – елементів – 36; d – елементів – 40;f – елементів – 28.

Слайд #19
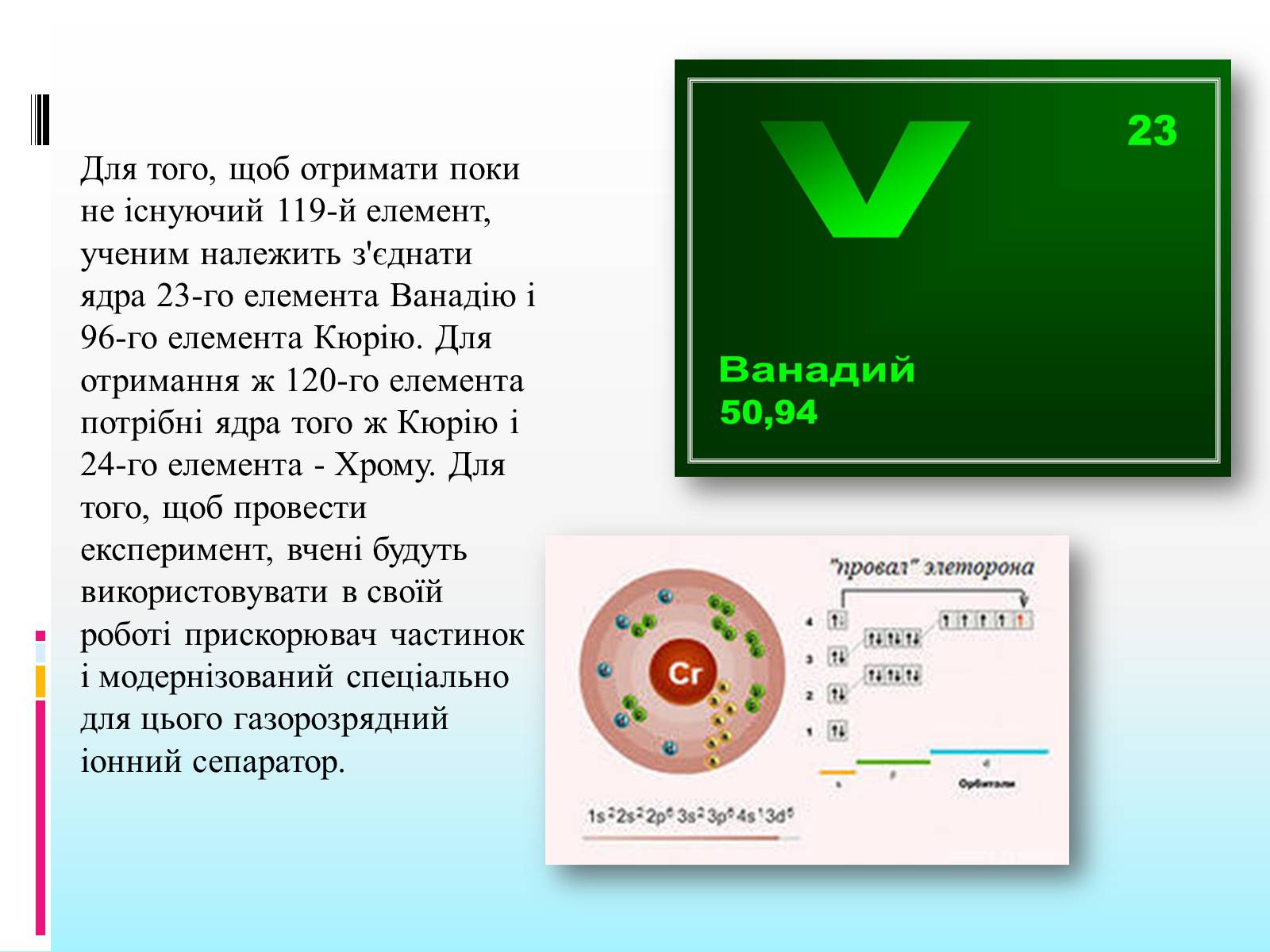
Для того, щоб отримати поки не існуючий 119-й елемент, ученим належить з'єднати ядра 23-го елемента Ванадію і 96-го елемента Кюрію. Для отримання ж 120-го елемента потрібні ядра того ж Кюрію і 24-го елемента - Хрому. Для того, щоб провести експеримент, вчені будуть використовувати в своїй роботі прискорювач частинок і модернізований спеціально для цього газорозрядний іонний сепаратор.
Слайд #20
Дякуємо за увагу!
