- Головна
- Готові шкільні презентації
- Презентація на тему «Химические свойства и применение алкенов»
Презентація на тему «Химические свойства и применение алкенов»
265
Слайд #1
Химические свойства и применение алкенов
«Границ научному познанию и предсказанию предвидеть не возможно»
Д. И. Менделеев
«Границ научному познанию и предсказанию предвидеть не возможно»
Д. И. Менделеев

Слайд #2
Химические свойства алкенов
ПрисоединениеtГидрированиеtГалогенированиеtГидрогалогенированиеtГидратация
Полимеризация
Окисление
Горение
Каталитическое окисление
ПрисоединениеtГидрированиеtГалогенированиеtГидрогалогенированиеtГидратация
Полимеризация
Окисление
Горение
Каталитическое окисление

Слайд #3
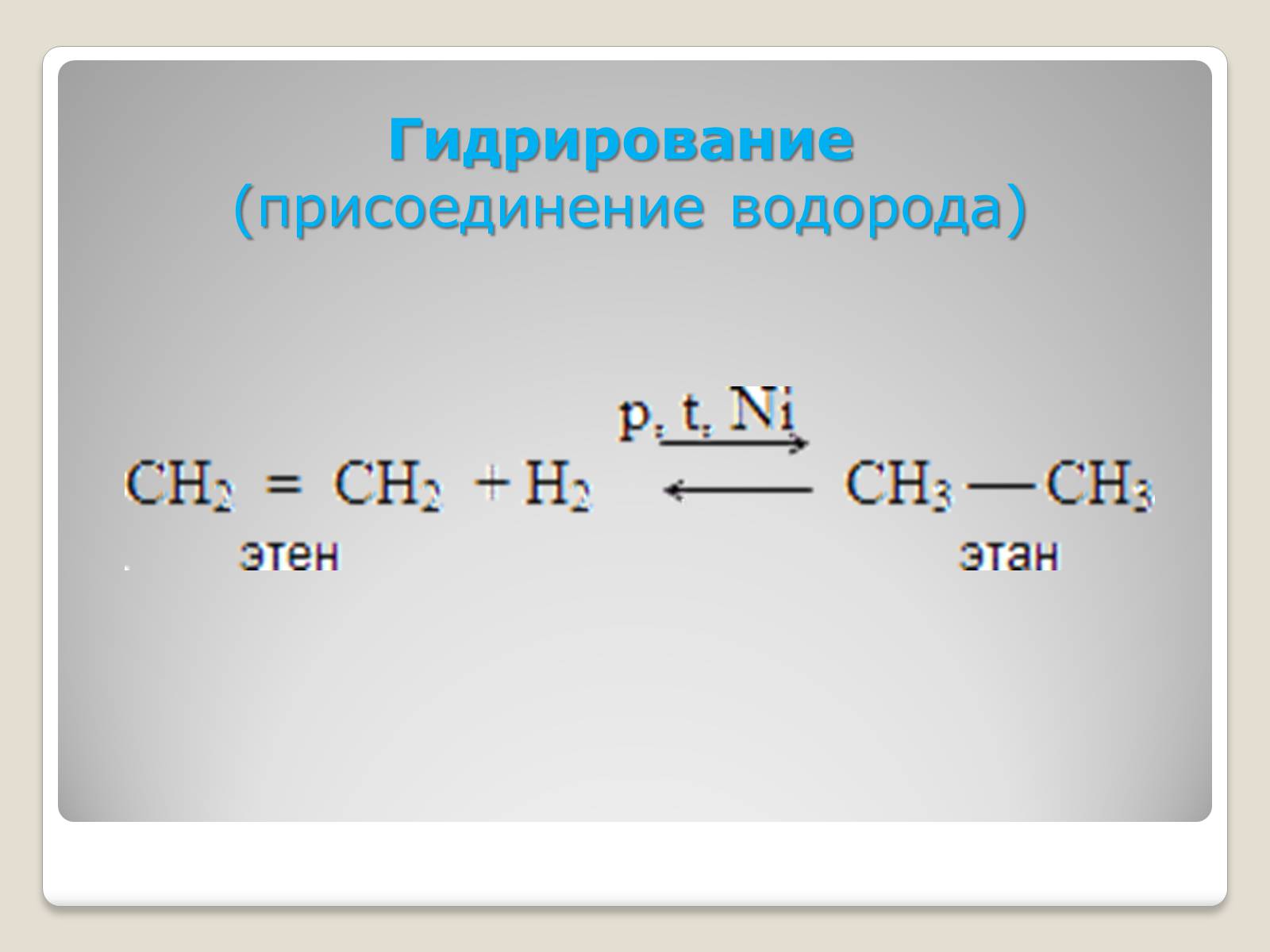
Гидрирование
(присоединение водорода)
(присоединение водорода)
Слайд #4
Гидрогалогенирование
(присоединение галогеноводородов)
(присоединение галогеноводородов)

Слайд #5
Галогенирование
(присоединение хлора, брома)
При использовании раствора брома в воде (бромной воды), имеющей желтовато-коричневую окраску, происходит ее обесцвечивание, что вы и наблюдали в ранее проведенном опыте.
В случае гомологов этилена важно выполнять условия проведения реакции галогенирования.
Например, при обычной температуре пропен вступает в реакцию присоединения хлора:
А при t 500oС идет замещение атомов водорода в метильной группе на атомы хлора:
(присоединение хлора, брома)
При использовании раствора брома в воде (бромной воды), имеющей желтовато-коричневую окраску, происходит ее обесцвечивание, что вы и наблюдали в ранее проведенном опыте.
В случае гомологов этилена важно выполнять условия проведения реакции галогенирования.
Например, при обычной температуре пропен вступает в реакцию присоединения хлора:
А при t 500oС идет замещение атомов водорода в метильной группе на атомы хлора:

Слайд #6
Рассмотрим механизм электрофильного присоединениябромоводорода к этену.
Реакция начинается с процесса диссоциации бромоводорода:
HBr → H+ + Br–
Катион водорода H+ атакует π-связь (как бы натыкается на выступающую из плоскости молекулы электронную плотность π-связи) и присоединяется к ней, образуя π-комплекс:
CH2 = CH2 + H+ → CH2 CH2
За счет π-электронной пары происходит образование ковалентной связи протона H+ с одним из атомов углерода по донорно-акцепторному механизму:
CH2 CH2 → +CH2 – CH3
Образовавшийся карбкатион +CH2 – CH3 присоединяет анион Br– :
+CH2 – CH3 + Br– → CH2Br – CH3
Реакция начинается с процесса диссоциации бромоводорода:
HBr → H+ + Br–
Катион водорода H+ атакует π-связь (как бы натыкается на выступающую из плоскости молекулы электронную плотность π-связи) и присоединяется к ней, образуя π-комплекс:
CH2 = CH2 + H+ → CH2 CH2
За счет π-электронной пары происходит образование ковалентной связи протона H+ с одним из атомов углерода по донорно-акцепторному механизму:
CH2 CH2 → +CH2 – CH3
Образовавшийся карбкатион +CH2 – CH3 присоединяет анион Br– :
+CH2 – CH3 + Br– → CH2Br – CH3

Слайд #7
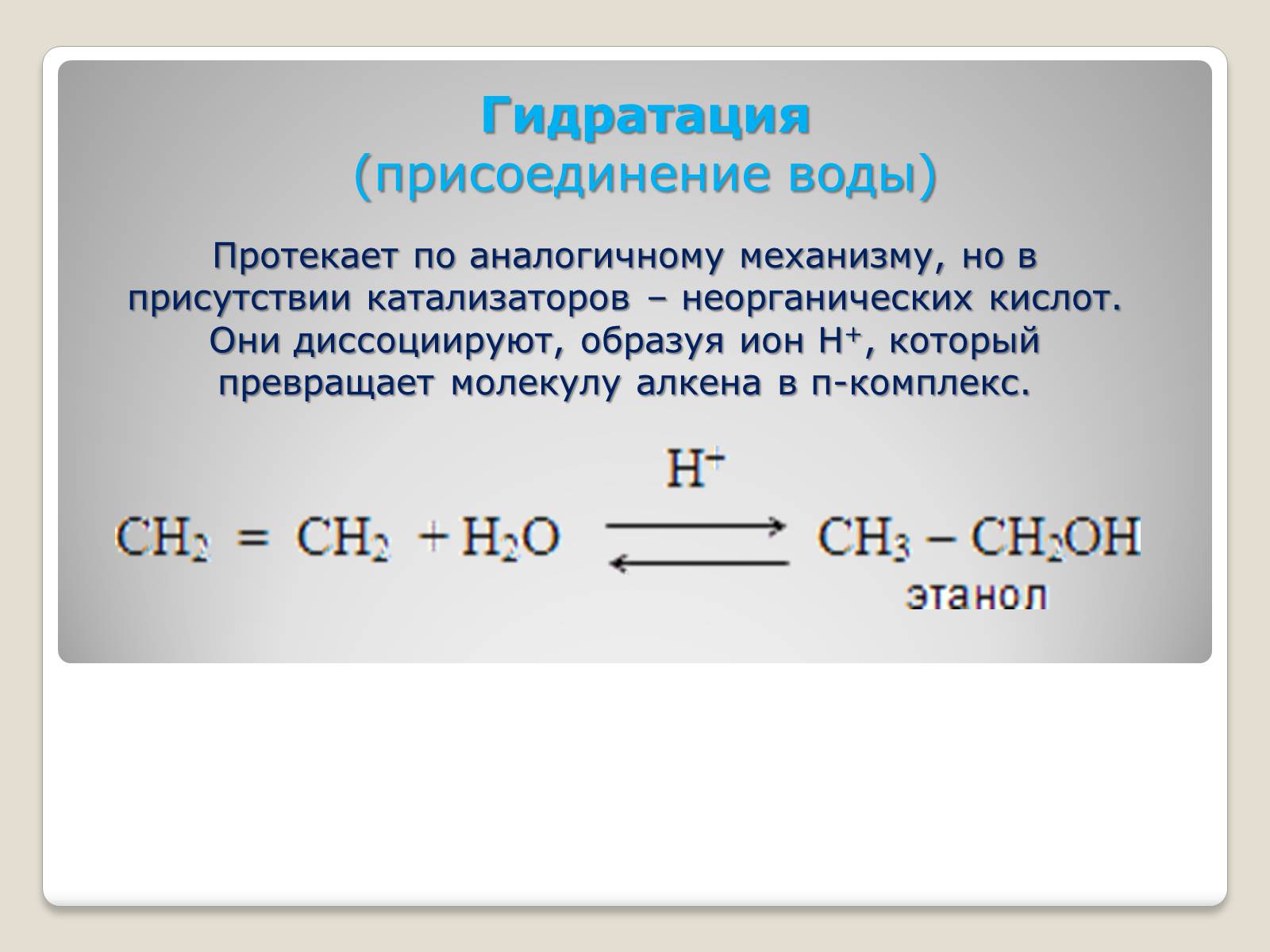
Гидратация
(присоединение воды)
Протекает по аналогичному механизму, но в присутствии катализаторов – неорганических кислот. Они диссоциируют, образуя ион Н+, который превращает молекулу алкена в π-комплекс.
(присоединение воды)
Протекает по аналогичному механизму, но в присутствии катализаторов – неорганических кислот. Они диссоциируют, образуя ион Н+, который превращает молекулу алкена в π-комплекс.
Слайд #8
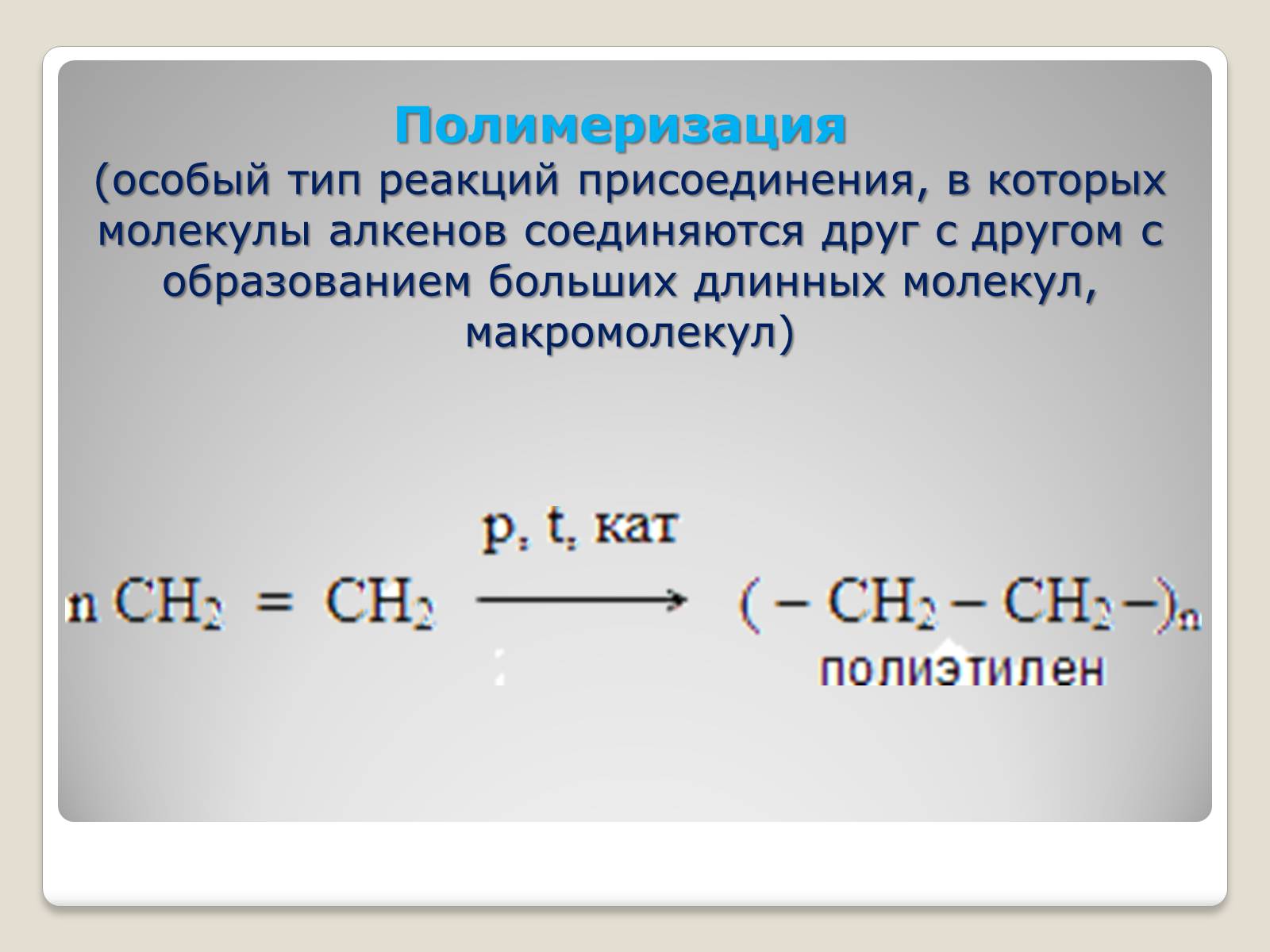
Полимеризация
(особый тип реакций присоединения, в которых молекулы алкенов соединяются друг с другом с образованием больших длинных молекул, макромолекул)
(особый тип реакций присоединения, в которых молекулы алкенов соединяются друг с другом с образованием больших длинных молекул, макромолекул)
Слайд #9
Горение
Поскольку элементный состав алкенов тот же, что и у предельных углеводородов, то они имеют общее свойство – горючесть. При поджигании алкены горят.
Поскольку элементный состав алкенов тот же, что и у предельных углеводородов, то они имеют общее свойство – горючесть. При поджигании алкены горят.

Слайд #10
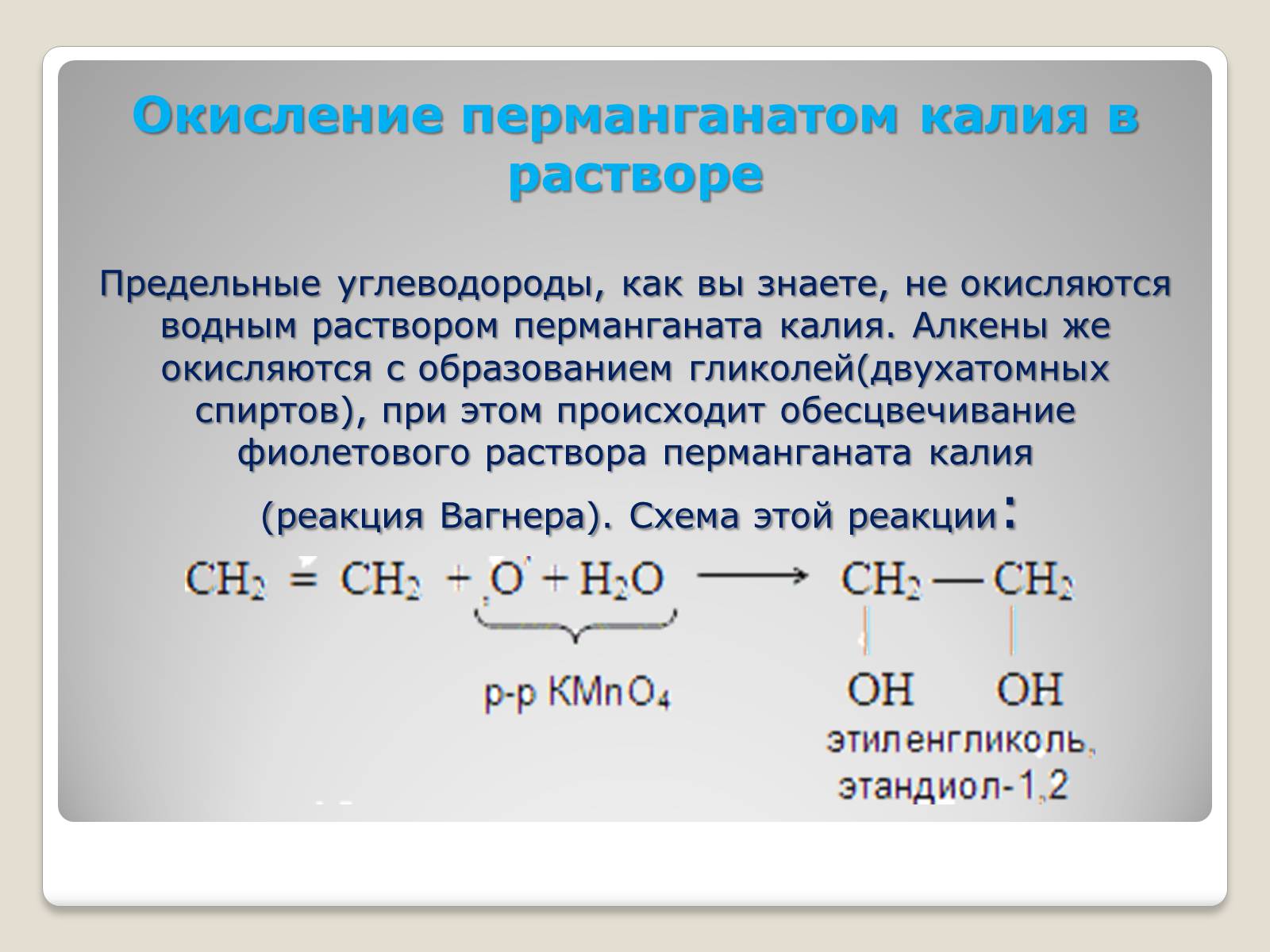
Окисление перманганатом калия в растворе
Предельные углеводороды, как вы знаете, не окисляются водным раствором перманганата калия. Алкены же окисляются с образованием гликолей(двухатомных спиртов), при этом происходит обесцвечивание фиолетового раствора перманганата калия
(реакция Вагнера). Схема этой реакции:
Предельные углеводороды, как вы знаете, не окисляются водным раствором перманганата калия. Алкены же окисляются с образованием гликолей(двухатомных спиртов), при этом происходит обесцвечивание фиолетового раствора перманганата калия
(реакция Вагнера). Схема этой реакции:
Слайд #11
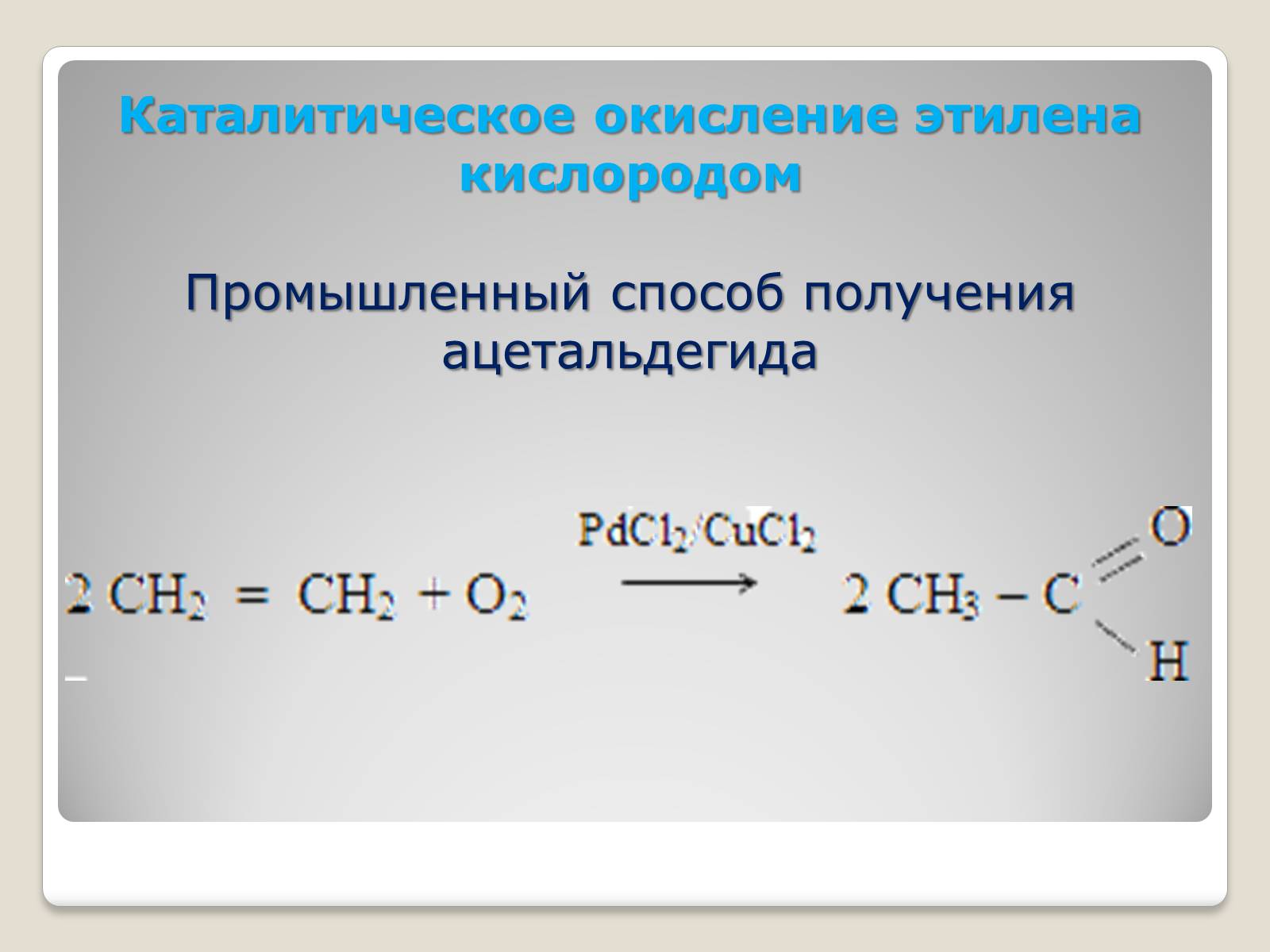
Каталитическое окисление этилена кислородом
Промышленный способ получения ацетальдегида
Промышленный способ получения ацетальдегида
Слайд #12
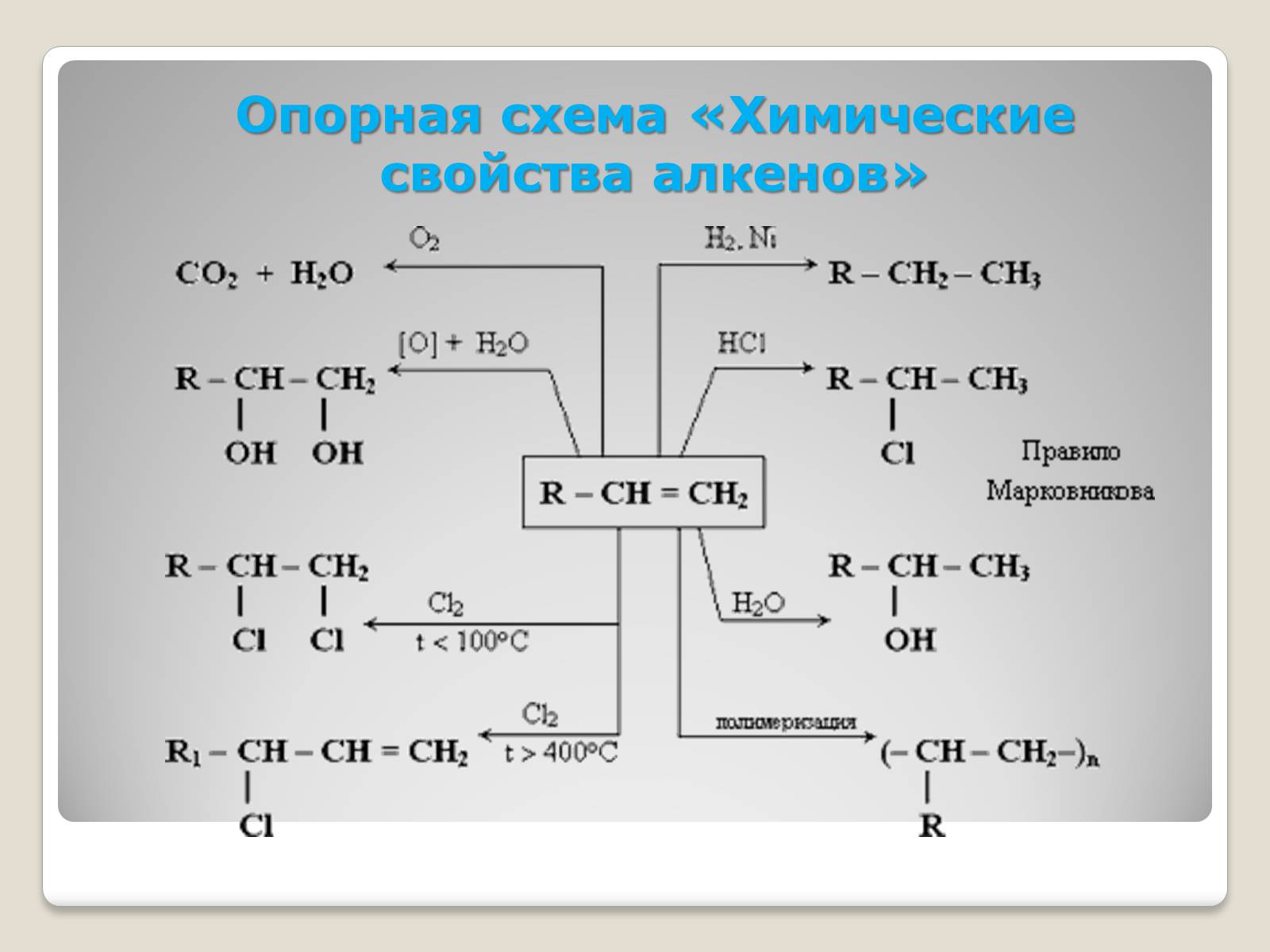
Опорная схема «Химические свойства алкенов»
Слайд #13
Применение алкенов
Изучая химические свойства алкенов, вы, очевидно, поняли, что благодаря высокой реакционной способности они являются ценным сырьем для химической промышленности. На их основе получают сотни практически важных продуктов и материалов.
Изучая химические свойства алкенов, вы, очевидно, поняли, что благодаря высокой реакционной способности они являются ценным сырьем для химической промышленности. На их основе получают сотни практически важных продуктов и материалов.

Слайд #14
Выполнил:Строкань Владислав 11-В

Слайд #15
Литература:
http://alhimikov.net/organikbook/alcen_01.html
http://old.internet-school.ru/demo/530384?page=1
http://ru.wikipedia.org/wiki/%D0%90%D0%BB%D0%BA%D0%B5%D0%BD%D1%8B
http://images.yandex.ua/?uinfo=ww-1263-wh-917-fw-0-fh-598-pd-1
http://alhimikov.net/organikbook/alcen_01.html
http://old.internet-school.ru/demo/530384?page=1
http://ru.wikipedia.org/wiki/%D0%90%D0%BB%D0%BA%D0%B5%D0%BD%D1%8B
http://images.yandex.ua/?uinfo=ww-1263-wh-917-fw-0-fh-598-pd-1
