- Головна
- Готові шкільні презентації
- Презентація на тему «Загальна характеристика оксидів»
Презентація на тему «Загальна характеристика оксидів»
176
Слайд #1
8 клас:Тема”Загальна характеристика оксидів.”
Верхівцевький НВК.
Учитель хімії Кукса Наталія Миколаївна
Верхівцевький НВК.
Учитель хімії Кукса Наталія Миколаївна

Слайд #2
Мета.
На прикладі найпростіших за складом і будовою хімічних сполук почати вивчення основних класів неорганічних сполук. Закріпити навички складання формул оксидів та називати їх. Поглибити знання про реакції сполучення, їх роль в утворенні оксидів.Розібрати властивості та роль оксидів в природі та нашому житті
На прикладі найпростіших за складом і будовою хімічних сполук почати вивчення основних класів неорганічних сполук. Закріпити навички складання формул оксидів та називати їх. Поглибити знання про реакції сполучення, їх роль в утворенні оксидів.Розібрати властивості та роль оксидів в природі та нашому житті

Слайд #3
Цілі:
Склад оксидів та назви
Знаходження в природі
Фізичні властивості
Хімічні властивості
Застосування
Значення для життєдіяльності
Склад оксидів та назви
Знаходження в природі
Фізичні властивості
Хімічні властивості
Застосування
Значення для життєдіяльності

Слайд #4
Загальна формула оксидів
Еn Оm
Еn Оm

Слайд #5
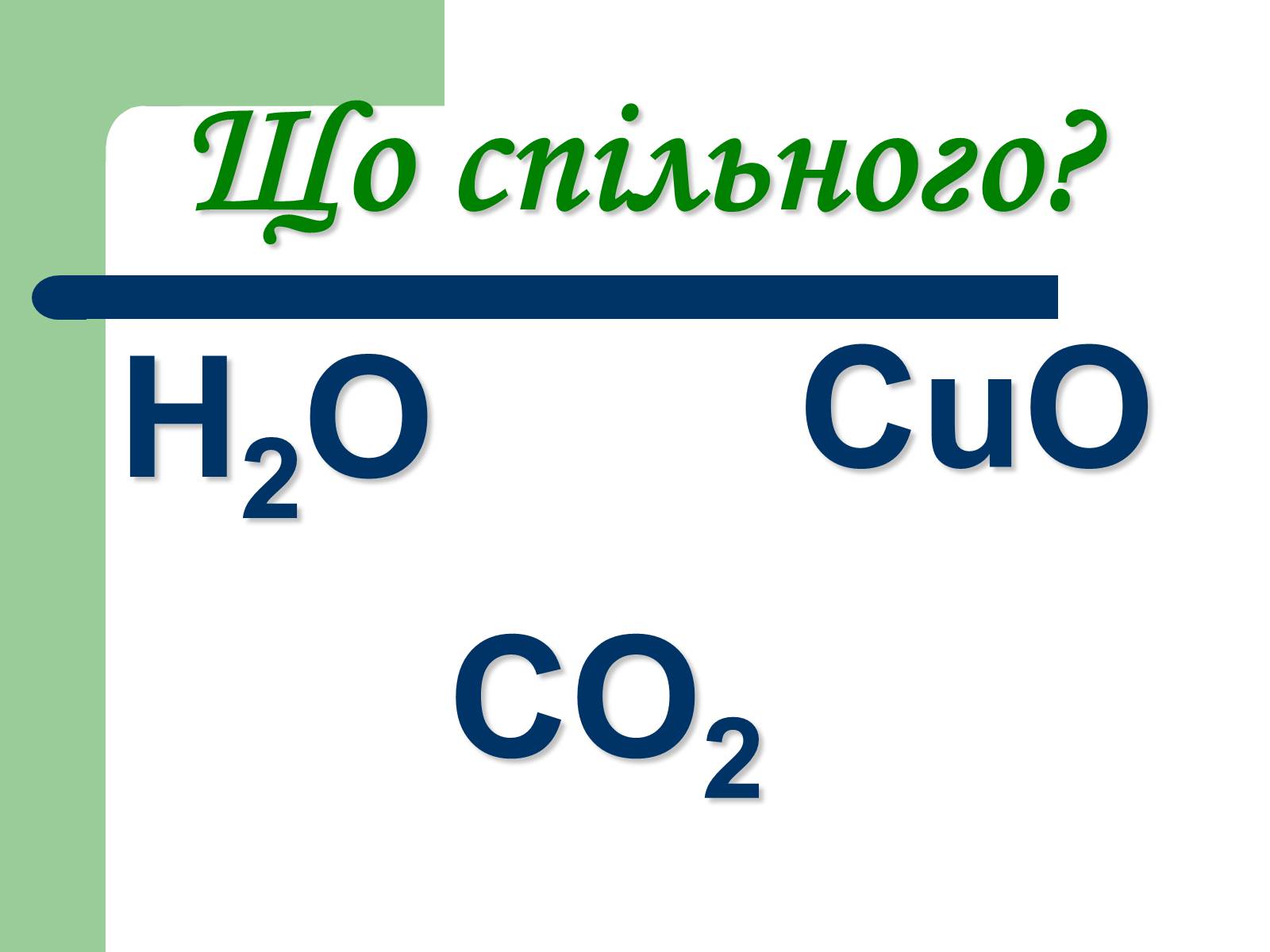
Н2О
CO2
CuO
Що спільного?
CO2
CuO
Що спільного?
Слайд #6
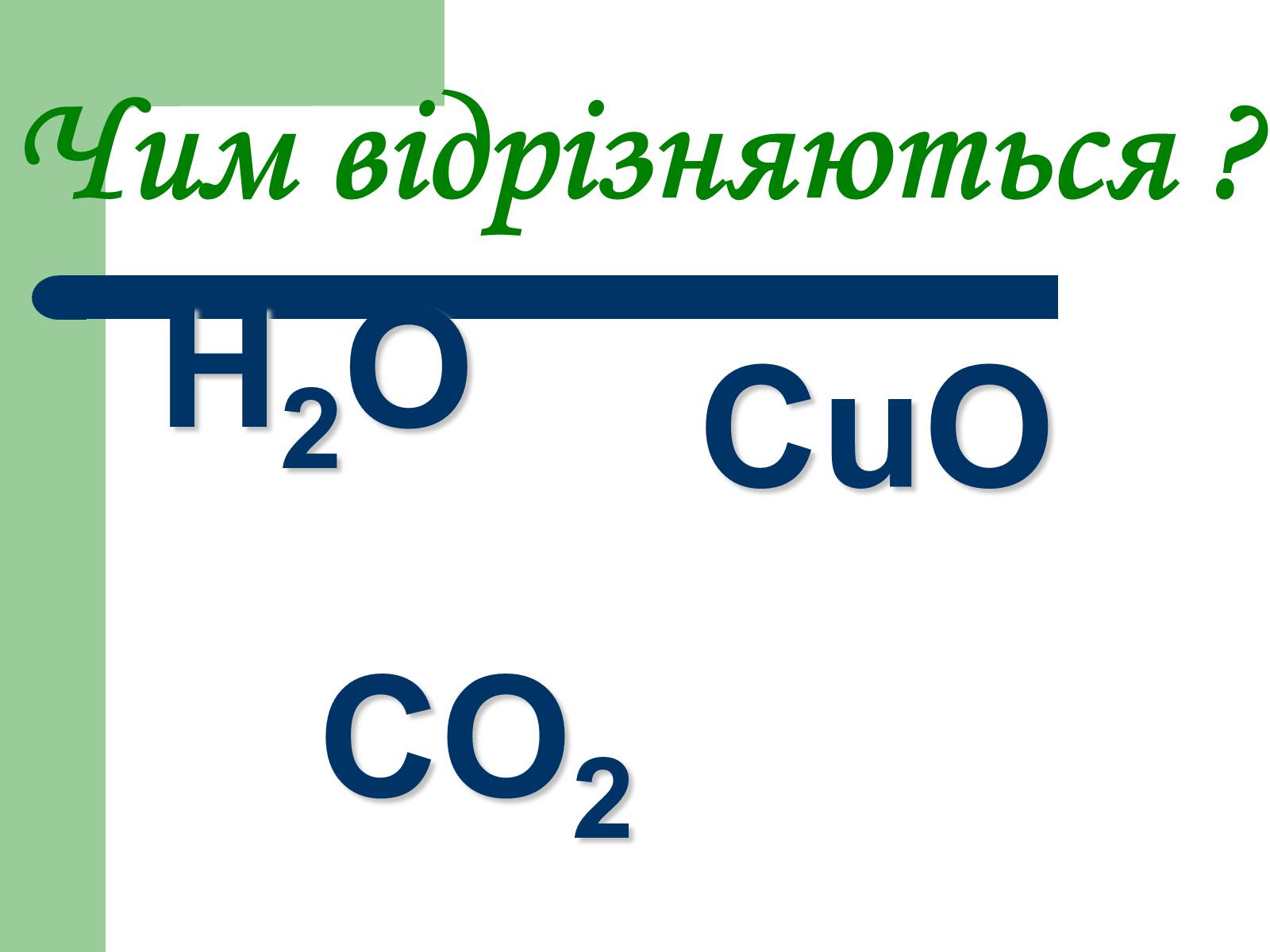
Н2О
CO2
CuO
Чим відрізняються ?
CO2
CuO
Чим відрізняються ?
Слайд #7
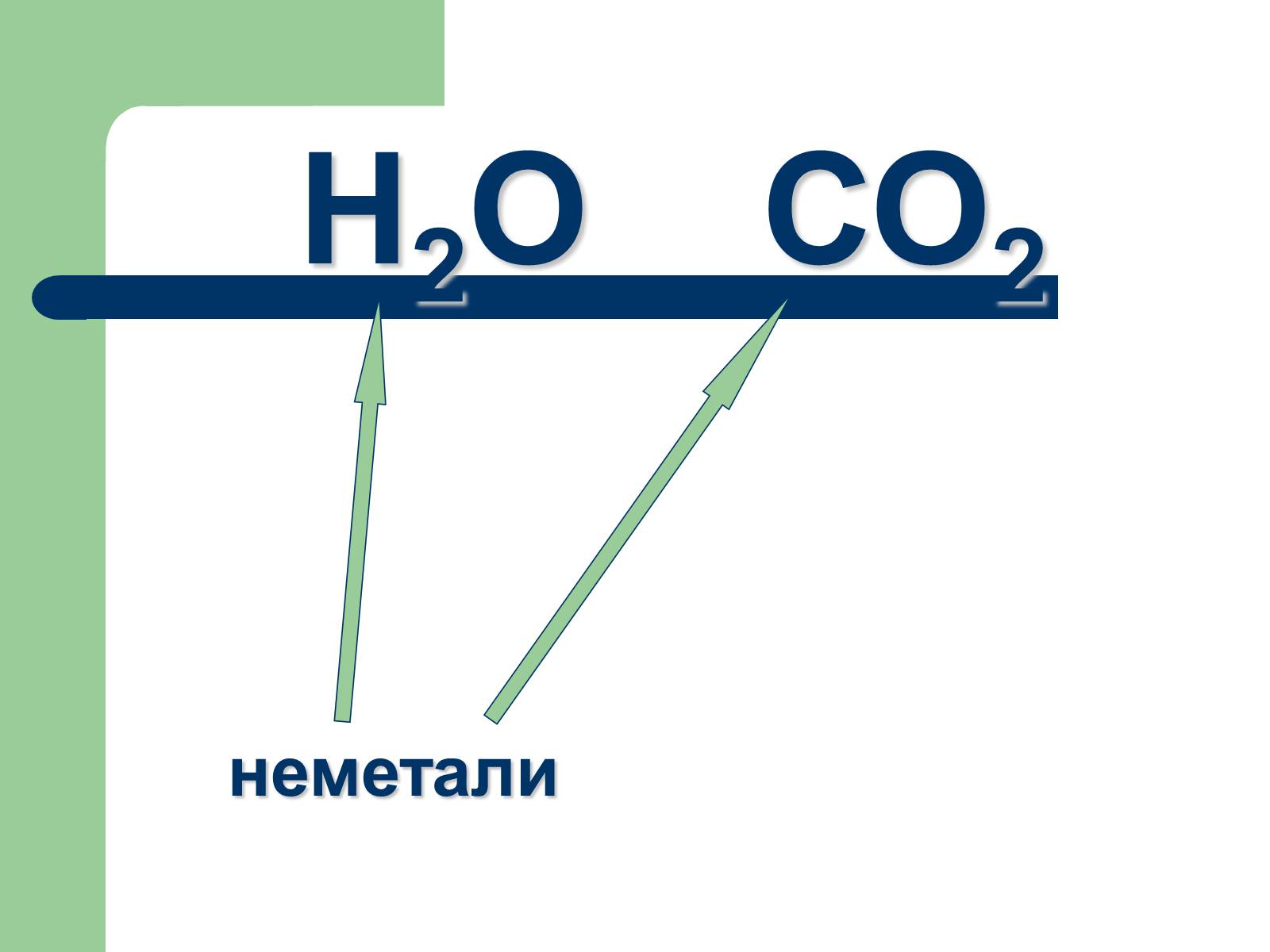
Н2О СО2
неметали
неметали
Слайд #8
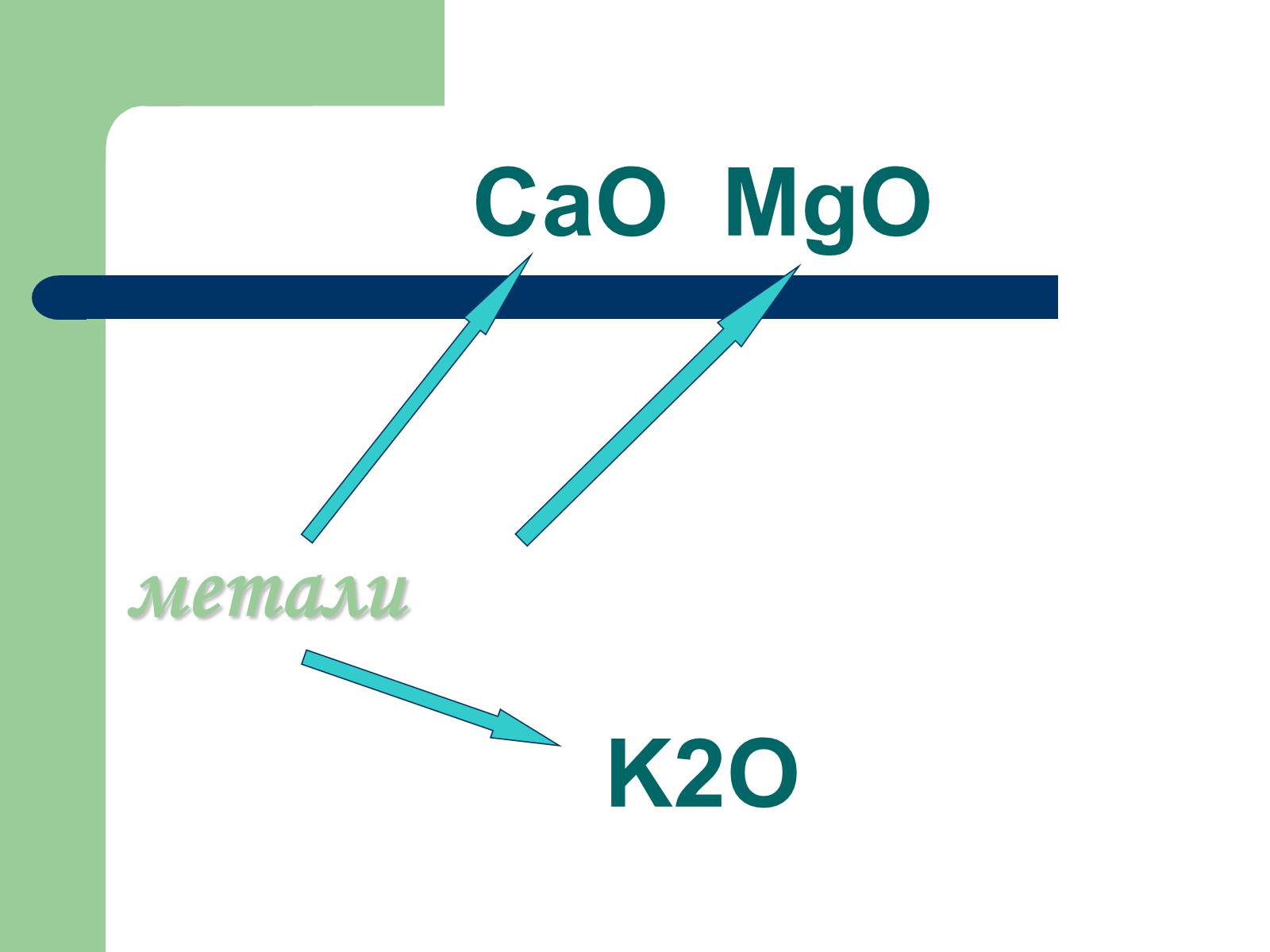
СаО MgO
K2O
метали
K2O
метали
Слайд #9
Амфотерність
Амфотерність –здатність елементів виявляти подвійні властивості.
Be Al Fe Zn
Приклади
Al2O3 Fe2O3
ZnO
Амфотерність –здатність елементів виявляти подвійні властивості.
Be Al Fe Zn
Приклади
Al2O3 Fe2O3
ZnO

Слайд #10
Утворення назви оксидів
Назва металу чи неметалу
+
Валентність елемента
+
Слово оксид
Назва металу чи неметалу
+
Валентність елемента
+
Слово оксид

Слайд #11
ВОДАH2O - гідроген оксид

Слайд #12
Вуглекислий газ CO2 - Карбон (IV)оксид

Слайд #13
Бурий газ NO2 - Нітроген (IV) оксид

Слайд #14
Кварц SiO2 -Силіцій(IV)оксид

Слайд #15
Природні сполуки оксиду алюмінію:
боксит, корунд, рубін, сапфіри
Алюміній (ІІІ)оксид – Al2O3
боксит, корунд, рубін, сапфіри
Алюміній (ІІІ)оксид – Al2O3

Слайд #16
Червоний та бурий залізнякФерум(ІІІ)оксид Fe2O3

Слайд #17
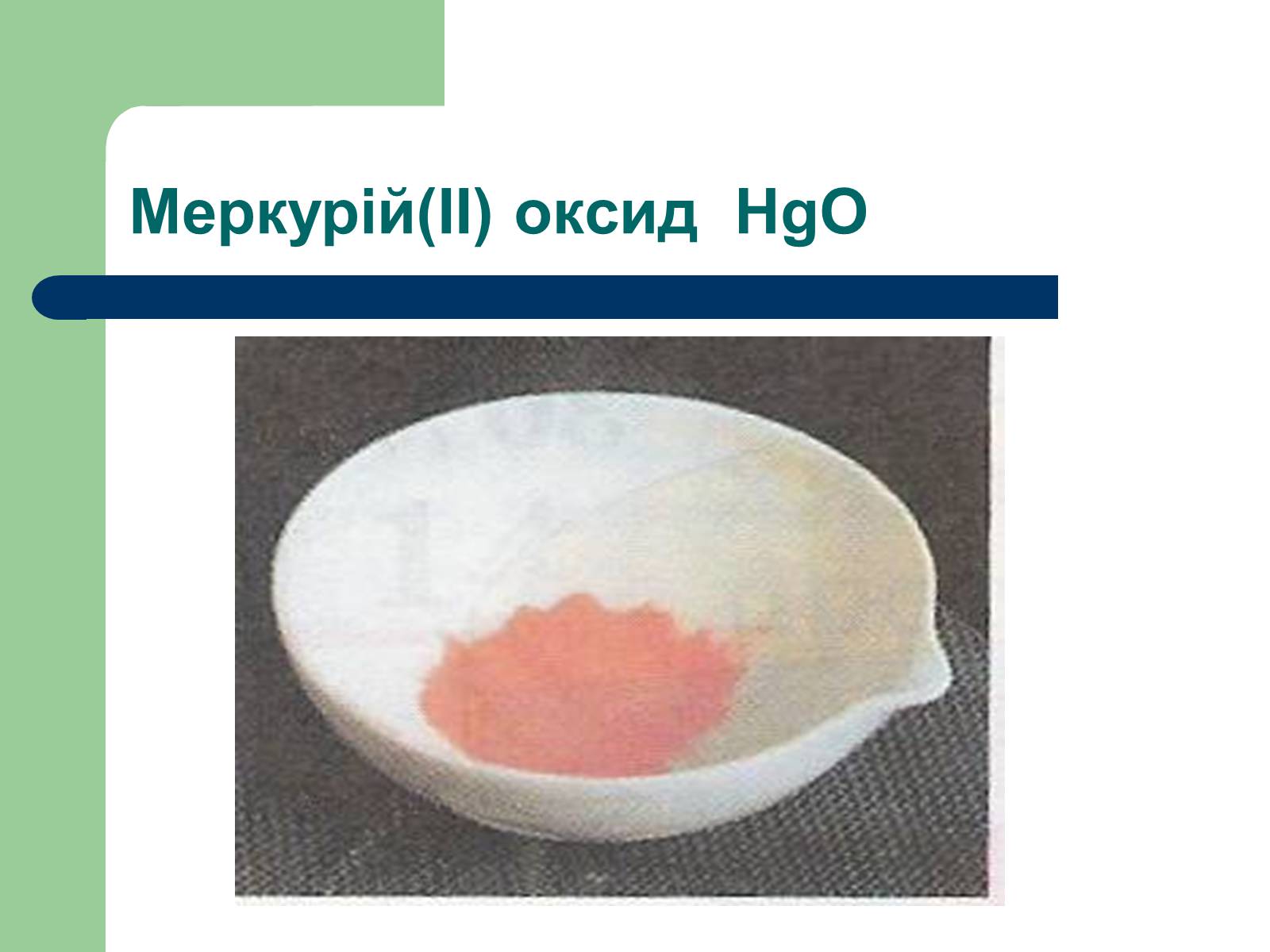
Меркурій(ІІ) оксид HgO
Слайд #18
Купрум оксид Cu2O

Слайд #19
Купрум(ІІ)оксид CuO

Слайд #20
ПіролюзитМанган (IV)оксид MnO2

Слайд #21
Хром(ІІІ)оксид-Cr2O3

Слайд #22
Хром (VI) оксид CrO3

Слайд #23
Плюмбум(ІІ)оксид PbO

Слайд #24
Фізичні властивості основних та амфотерних оксидів
Тверді
Кристалічні
Різнокольорові
Тверді
Кристалічні
Різнокольорові

Слайд #25
Фізичні властивості кислотних оксидів.
Можуть бути:
Твердими( SiO2,P2 O5)
Рідкими (H2O)
Газоподібні (СO2, SO2,NO)
Можуть бути:
Твердими( SiO2,P2 O5)
Рідкими (H2O)
Газоподібні (СO2, SO2,NO)

Слайд #26
Хімічні властивості основних оксидів
Взаємодіють з водою з утворенням основ
CaO+H2O=Ca(OH)2
Na2O+H2O=2 NaOH
Взаємодіють з водою з утворенням основ
CaO+H2O=Ca(OH)2
Na2O+H2O=2 NaOH

Слайд #27
Хімічні властивості кислотних оксидів
Взаємодіють з водою з утворенням кислот
СO2+H2O=H2CO3
SO3+H2O=H2SO4
Взаємодіють з водою з утворенням кислот
СO2+H2O=H2CO3
SO3+H2O=H2SO4

Слайд #28
Взаємодіють між собою з утворенням солей
CaO+CO2=CaCO3
MgO+SO2=MgSO3
CaO+CO2=CaCO3
MgO+SO2=MgSO3

Слайд #29
Основні оксиди взаємодіють з кислотами
СaO+ 2HCl=CaCl2+H2O
Na2O+H2SO4=Na2SO4+H2O
Утворюється сіль та вода
СaO+ 2HCl=CaCl2+H2O
Na2O+H2SO4=Na2SO4+H2O
Утворюється сіль та вода

Слайд #30
Кислотні оксиди взаємодіють з основами
СO2+2KOH=K2CO3+H2O
SO3+2NaOH=Na2SO4+H2O
Утворюється сіль та вода
СO2+2KOH=K2CO3+H2O
SO3+2NaOH=Na2SO4+H2O
Утворюється сіль та вода

Слайд #31
Знаходження
оксидів в природі
та значення
для життєдіяльності
оксидів в природі
та значення
для життєдіяльності

Слайд #32
«Первое начало и сущность всего – …»tФалес из Милета (VI в. до н.э.)
Вгадай що знаходиться в першій шкатулці,?
Вгадай що знаходиться в першій шкатулці,?

Слайд #33
Вода
Вода – це найдивовижніша, найпоширеніша і найнеобхідніша речовина на нашій планеті.
Вода – джерело життя на Землі, сировина для промисловості, джерело енергії, чинник, що визначає погоду, клімат Землі. Три чверті земної поверхні вкрито водою, що утворює океани, моря, ріки та озера.
Вода – це найдивовижніша, найпоширеніша і найнеобхідніша речовина на нашій планеті.
Вода – джерело життя на Землі, сировина для промисловості, джерело енергії, чинник, що визначає погоду, клімат Землі. Три чверті земної поверхні вкрито водою, що утворює океани, моря, ріки та озера.

Слайд #34
Вода в природі

Слайд #35
Вода в природі

Слайд #36
Складіть асоціативний ряд до слова «вода»

Слайд #37
Акваріум

Слайд #38
Акваторія

Слайд #39
Акваланг

Слайд #40
Акварель

Слайд #41
Газ, необхідний
рослинам для
фотосинтеза
А що в цій шкатулці ?
рослинам для
фотосинтеза
А що в цій шкатулці ?

Слайд #42
Вуглекислий газ
До складу повітря входить карбон(IV) оксид СО2 (вуглекислий газ), об'ємна частка якого в повітрі становить 0,3 %.
До складу повітря входить карбон(IV) оксид СО2 (вуглекислий газ), об'ємна частка якого в повітрі становить 0,3 %.

Слайд #43
«…На рукомойнике моем
позеленела медь,
Но так играет луч на нем,
что весело глядеть…»
А. Ахматова
А що в останій шкатулці ?
позеленела медь,
Но так играет луч на нем,
что весело глядеть…»
А. Ахматова
А що в останій шкатулці ?

Слайд #44
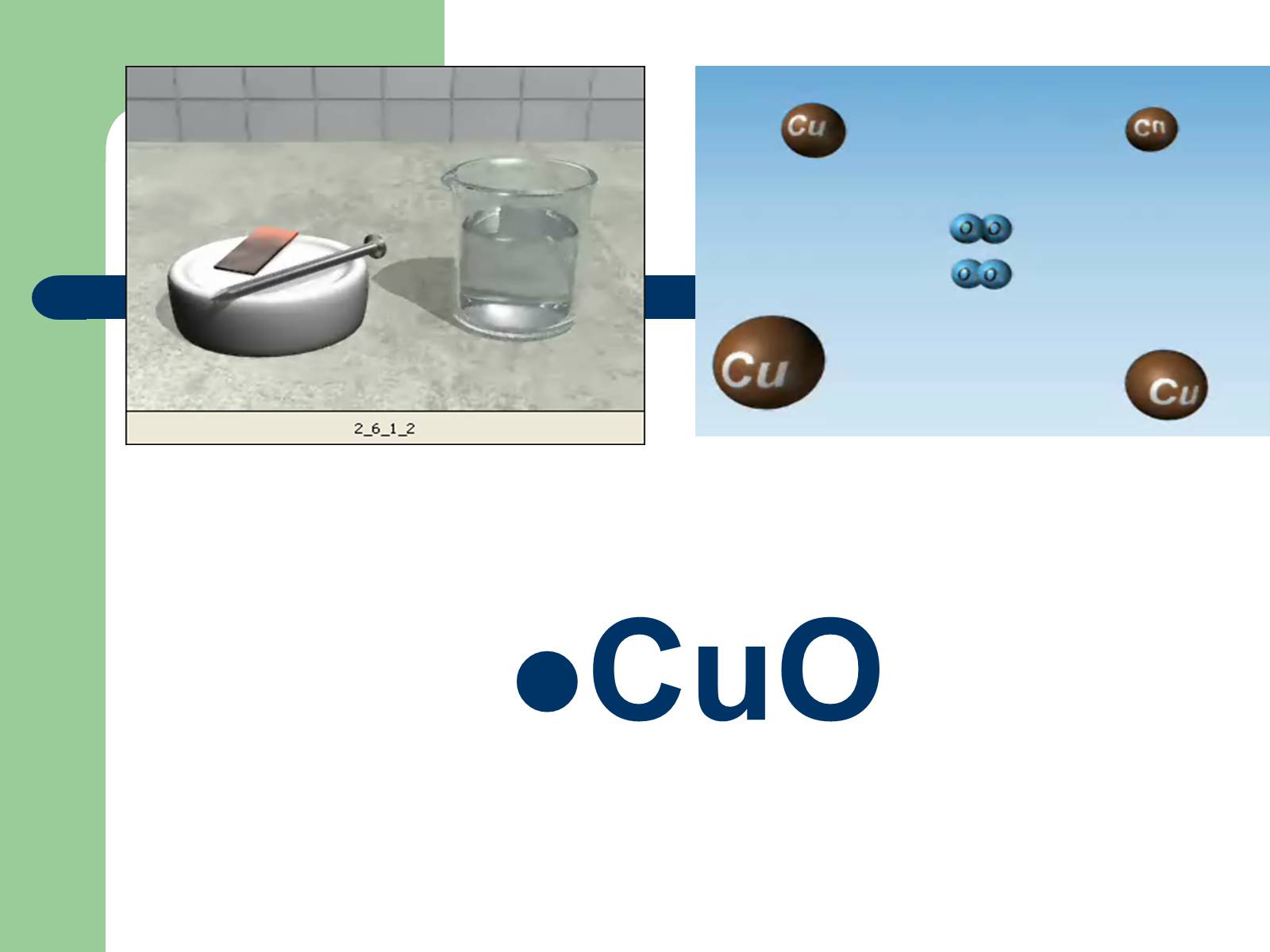
CuO
Слайд #45
Складіть формули оксидів елементів
Магнію
Калію
Алюмінію
Фосфору(V)
Хлору (VII )
Заліза (III)
карбону (IV)
сульфуру (VI)
Випишіть в два стовбчика оксиди металів і неметалів.
Магнію
Калію
Алюмінію
Фосфору(V)
Хлору (VII )
Заліза (III)
карбону (IV)
сульфуру (VI)
Випишіть в два стовбчика оксиди металів і неметалів.

Слайд #46
Розрахуйте:
1.Массу 1літру вуглекислого газау(н.у.).
2.Об'єм 3,4г амміаку.(н.у.)(NH3)
3.Скільки міститься молекул в 2 г хлороводню?(HCl)
1.Массу 1літру вуглекислого газау(н.у.).
2.Об'єм 3,4г амміаку.(н.у.)(NH3)
3.Скільки міститься молекул в 2 г хлороводню?(HCl)

Слайд #47
Домашнє завдання
Прочитати § 5,9 виконати завдання
№ 49,52,84
Прочитати § 5,9 виконати завдання
№ 49,52,84
